บทความวิชาการ เดือนพฤษภาคม 2569
บทบาทของการให้ยาเคมีบำบัดร้อนในช่องท้อง
(Hyperthermic Intraperitoneal Chemotherapy หรือ HIPEC)
สำหรับการรักษามะเร็งนรีเวช
ผศ.ดร.นพ.มรุต ญาณารณพ
งานมะเร็งนรีเวชวิทยา กลุ่มงานสูตินรีเวชศาสตร์ โรงพยาบาลราชวิถี
มะเร็งที่แพร่กระจายสู่เยื่อบุช่องท้อง เช่น มะเร็งรังไข่ มะเร็งกระเพาะอาหาร มะเร็งไส้ติ่ง และอื่นๆ มักมีพยากรณ์โรคไม่ดีและตอบสนองต่อเคมีบำบัดทางหลอดเลือดดำจำกัด (1) การให้ยาเคมีบำบัดร้อนในช่องท้อง (hyperthermic intraperitoneal chemotherapy หรือ HIPEC) ร่วมกับการผ่าตัดลดมวลเนื้องอก (cytoreductive surgery หรือ CRS) หรือที่เรียกว่า “การผ่าตัด HIPEC” เป็นแนวทางการรักษามะเร็งแบบเฉพาะที่ที่ช่วยลดการกลับเป็นซ้ำของโรคและเพิ่มอัตราการรอดชีวิต แต่เป็นหัตถการที่ซับซ้อนและมีความเสี่ยงสูง จึงต้องคัดเลือกผู้ป่วยอย่างเหมาะสม
หลักการทางเภสัชวิทยาของการให้ยาเคมีบำบัดทางช่องท้อง (Intraperitoneal Chemotherapy)
เยื่อบุช่องท้อง ทำหน้าที่เป็น peritoneal–plasma barrier ส่งผลให้ยาเคมีบำบัดที่ให้ทางหลอดเลือดดำมีการซึมผ่านเข้าสู่ช่องท้องได้จำกัด (2) ขณะที่การให้ยาเคมีบำบัดทางช่องท้อง ทำให้ได้ความเข้มข้นยาเฉพาะที่สูงและลดผลข้างเคียงต่อร่างกาย ยาซึมผ่านเข้าสู่เนื้อเยื่อได้ลึกเพียงประมาณ 1–3 มม. (3, 4) ความร้อนที่อุณหภูมิ 41–43 °C เหมาะสมต่อการเสริมฤทธิ์ของยาเคมีบำบัด (5, 6) ช่วยเพิ่มการซึมผ่านของยา เพิ่มการสะสมของยาในเซลล์มะเร็งมากกว่าเซลล์ปกติ และรบกวนกลไกการอยู่รอดของเซลล์มะเร็ง ยาเคมีบำบัดที่ใช้ใน HIPEC มักเป็นยาที่ออกฤทธิ์ไม่จำเพาะต่อวัฏจักรเซลล์ สามารถคงอยู่ในช่องท้องได้ในระดับความเข้มข้นสูงกว่าพลาสมา และมีคุณสมบัติในการออกฤทธิ์เสริมกับความร้อนได้ดี ยาเคมีบำบัดที่ใช้บ่อยใน HIPEC ได้แก่ cisplatin, carboplatin, oxaliplatin, mitomycin C และ doxorubicin (7, 8) HIPEC นำมาใช้ร่วมกับการผ่าตัดลดมวลเนื้องอก (9) โดยมีเป้าหมายเพื่อมุ่งกำจัดทั้งก้อนมะเร็งที่มองเห็นได้โดยการผ่าตัด และเซลล์มะเร็งระดับจุลภาคที่ยังหลงเหลืออยู่โดยการให้ยาเคมีบำบัดที่ถูกทำให้ร้อนหมุนเวียนภายในช่องท้อง
บทบาทของการให้ยาเคมีบำบัดร้อนในช่องท้องสำหรับการรักษามะเร็งนรีเวช
การผ่าตัด HIPEC เป็นแนวทางการรักษาที่มีบทบาทสำคัญเพิ่มขึ้นในการรักษามะเร็งนรีเวช มีบทบาทเด่นที่สุดในมะเร็งรังไข่ชนิดเยื่อบุผิว ซึ่งมีการแพร่กระจายสู่เยื่อบุช่องท้องบ่อยและมีอัตราการกลับเป็นซ้ำสูง แม้ได้รับการรักษามาตรฐานแล้วก็ตาม สำหรับมะเร็งนรีเวชชนิดอื่น เช่น มะเร็งรังไข่ชนิด sex cord-stromal มะเร็งเยื่อบุโพรงมดลูก และมะเร็งปากมดลูก หลักฐานเชิงประจักษ์ยังจำกัด (10)
บทบาทของการผ่าตัด HIPEC สำหรับการรักษามะเร็งรังไข่ชนิดเยื่อบุผิวในกรณีต่าง ๆ
-
HIPEC ในผู้ป่วยมะเร็งรังไข่ชนิดเยื่อบุผิวระยะลุกลามที่ผ่าตัดลดมวลเนื้องอกครั้งแรก (primary CRS) บทบาทของ HIPEC ยังไม่ชัดเจน แม้ว่าการศึกษาย้อนหลังบางฉบับจะรายงานผลลัพธ์การรอดชีวิตที่ดีขึ้น (11, 12, 13) แต่การศึกษา KOV-HIPEC-01 ซึ่งเป็นการทดลองแบบสุ่มและมีกลุ่มควบคุม ไม่พบประโยชน์ด้านการรอดชีวิตของ HIPEC อย่างชัดเจน (14) ดังนั้น ปัจจุบันยังไม่แนะนำให้ใช้ HIPEC เป็นมาตรฐานในบริบทนี้ และควรพิจารณาเฉพาะในงานวิจัยทางคลินิก
-
HIPEC ในผู้ป่วยมะเร็งรังไข่ชนิดเยื่อบุผิวระยะลุกลามที่ได้รับยาเคมีบำบัดเสริมก่อนผ่าตัด (neoadjuvant chemotherapy หรือ NAC) และผ่าตัดลดมวลเนื้องอกระหว่างให้ยาเคมีบำบัด (interval CRS หรือ Interval debulking surgery, IDS) บริบทนี้มีหลักฐานมีหลักฐานเชิงประจักษ์สนับสนุนชัดเจนที่สุด การศึกษา OVHIPEC-1 แสดงให้เห็นถึงประสิทธิผลของ HIPEC ร่วมกับการผ่าตัด IDS เปรียบเทียบการผ่าตัด IDS เพียงอย่างเดียวในผู้ป่วยมะเร็งรังไข่ระยะลุกลาม พบว่าค่ามัธยฐานระยะเวลารอดชีวิตโดยปราศจากความคืบหน้าของโรคเท่ากับ 2 เดือน เปรียบเทียบกับ 10.7 เดือน (HR: 0.66; 95% CI: 0.50–0.87; p = 0.03) และค่ามัธยฐานระยะเวลารอดชีวิตโดยรวมเท่ากับ 45.7 เดือน เปรียบเทียบกับ 33.9 เดือนตามลำดับ (HR: 0.67; 95% CI: 0.48–0.95; p = 0.02) ไม่พบความแตกต่างของภาวะแทรกซ้อนระดับรุนแรงอย่างมีนัยสำคัญ (15) การวิเคราะห์อภิมานยังสนับสนุนบทบาทของ HIPEC ในบริบทนี้ (16) แนะนำให้พิจารณาในผู้ป่วยมะเร็งรังไข่ชนิดเยื่อบุผิวระยะลุกลามที่ได้รับ NAC และสามารถผ่าตัด IDS ได้สำเร็จ (17, 18) โดยแนะนำให้การรักษาด้วย NAC 3-4 รอบ ตามด้วยการผ่าตัด IDS และ HIPEC โดยใช้ยา cisplatin 100 มก./ม.2 ที่อุณหภูมิ 42-43 °C เป็นระยะเวลา 60-90 นาที และให้ยาเคมีบำบัดเสริมหลังผ่าตัด (adjuvant chemotherapy) ต่อ (19)
-
HIPEC ร่วมกับการผ่าตัดลดมวลเนื้องอกครั้งที่สอง (secondary CRS) ในผู้ป่วยมะเร็งรังไข่ชนิดเยื่อบุผิวกลับเป็นซ้ำ บทบาทของ HIPEC ในมะเร็งรังไข่กลับเป็นซ้ำยังคงเป็นที่ถกเถียง การศึกษามีความหลากหลายและผลลัพธ์มีความขัดแย้งกัน (20, 21, 22) ดังนั้น ปัจจุบันยังไม่มีข้อบ่งชี้ให้ใช้ HIPEC เป็นมาตรฐานในผู้ป่วยมะเร็งรังไข่ระยะกลับเป็นซ้ำ แต่สามารถพิจารณาได้ในผู้ป่วยที่คัดเลือกอย่างเหมาะสม
กระบวนการผ่าตัดลดมวลเนื้องอกและให้ยาเคมีบำบัดร้อนในช่องท้องขณะผ่าตัด
- การประเมินและคัดเลือกผู้ป่วย ผู้ป่วยที่เหมาะสมสำหรับการรักษาด้วย HIPEC ควรมีสภาพร่างกายโดยรวมดี โรคยังจำกัดอยู่ภายในช่องท้อง และมีความเป็นไปได้ที่จะผ่าตัดเอาก้อนมะเร็งออกได้เกือบทั้งหมดหรือทั้งหมด
-
การสำรวจช่องท้องและประเมินการกระจายของโรคในเยื่อบุช่องท้อง ศัลยแพทย์จะทำการสำรวจช่องท้องโดยการผ่าตัดส่องกล้องเพื่อประเมิน peritoneal cancer index (23) ว่าผู้ป่วยมีโอกาสได้รับประโยชน์จากการผ่าตัดหรือไม่ เนื่องจากหากไม่สามารถกำจัดก้อนมะเร็งได้อย่างเพียงพอ การผ่าตัดอาจไม่ก่อให้เกิดประโยชน์ด้านการรอดชีวิต และกลับเพิ่มความเสี่ยงต่อภาวะแทรกซ้อนโดยไม่จำเป็น
-
การผ่าตัดลดมวลเนื้องอก เป็นการผ่าตัดที่มีเป้าหมายเพื่อกำจัดก้อนมะเร็งที่มองเห็นได้ทั้งหมด ประกอบด้วย การตัดอวัยวะที่มีการลุกลามของมะเร็ง (multi-visceral resection) ตลอดจนการตัดมดลูกและรังไข่ในผู้ป่วยมะเร็งนรีเวช และการเลาะเยื่อบุช่องท้อง (peritonectomy) (9) ดังนั้นการผ่าตัดนี้จึงเป็นการผ่าตัดที่ซับซ้อนและใช้เวลาในการผ่าตัดนานเฉลี่ย 8-12 ชั่วโมง การประเมินผลของการผ่าตัดจะประเมินโดยการใช้ completeness of cytoreduction หรือ CC score (24) ซึ่งมีความสัมพันธ์โดยตรงกับผลลัพธ์ด้านการพยากรณ์โรค การรอดชีวิต และการกลับเป็นซ้ำ
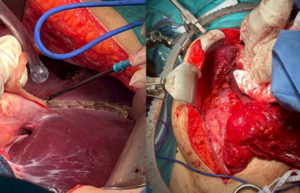
รูปที่ 1 แสดงการผ่าตัดเลาะเยื่อบุช่องท้องใต้กระบังลมขวา
-
การให้ยาเคมีบำบัดร้อนในช่องท้อง หลังจากผ่าตัดลดมวลเนื้องอกเสร็จสิ้นแล้ว ทำการใส่สายสำหรับหมุนเวียนสารละลายภายในช่องท้องและเชื่อมต่อกับเครื่องควบคุมการไหลและอุณหภูมิ ยาเคมีบำบัดจะถูกทำให้ร้อนขึ้นที่อุณหภูมิประมาณ 41–43 °C จากนั้นปล่อยให้ไหลไปหมุนเวียนภายในช่องท้องเป็นเวลา 60–90 นาที หลังจากนั้นทำการระบายสารเคมีบำบัดออกจากช่องท้อง ล้างช่องท้อง ใส่สายระบาย และปิดแผลผ่าตัด
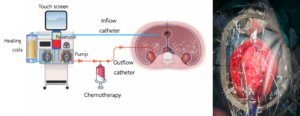
รูปที่ 2 แสดงการต่อสายสำหรับหมุนเวียนสารละลายภายในช่องท้อง
5. การดูแลหลังผ่าตัด ผู้ป่วยจะถูกส่งไปดูแลต่อในหอผู้ป่วยวิกฤตหรือหอผู้ป่วยที่มีการเฝ้าระวังอย่างใกล้ชิด
ภาวะแทรกซ้อนของการให้ยาเคมีบำบัดร้อนในช่องท้อง
การผ่าตัด HIPEC มีรายงานอุบัติการณ์ภาวะแทรกซ้อน ประมาณร้อยละ 30–40 ขณะที่อัตราการเสียชีวิต ประมาณร้อยละ 0–4 (25) ภาวะแทรกซ้อนที่พบบ่อย ได้แก่ การติดเชื้อในช่องท้องหรือแผลผ่าตัด การรั่วของลำไส้บริเวณรอยต่อ ภาวะลำไส้อุดตันหรือลำไส้หยุดทำงานชั่วคราว เลือดออก ลิ่มเลือดอุดตัน ตลอดจนภาวะแทรกซ้อนที่เกี่ยวข้องกับการระงับความรู้สึกและความปวดหลังผ่าตัด นอกจากนี้ อาจพบผลข้างเคียงจากยาเคมีบำบัด เช่น คลื่นไส้อาเจียน พิษต่อไต การกดไขกระดูก
บทสรุป
HIPEC เป็นการรักษาเฉพาะที่ที่มีประโยชน์ในผู้ป่วยมะเร็งรังไข่ชนิดเยื่อบุผิวระยะลุกลาม โดยเฉพาะในผู้ป่วยที่ได้รับ NAC และสามารถทำ IDS ได้สำเร็จ การเลือกผู้ป่วยอย่างเหมาะสมและการรักษาในศูนย์ที่มีความเชี่ยวชาญยังคงเป็นปัจจัยสำคัญต่อผลลัพธ์ของการรักษา
เอกสารอ้างอิง
-
Mohkam K, Passot G, Cotte E, Bakrin N, Gilly F-N, Ledochowski S, et al. Resectability of Peritoneal Carcinomatosis: Learnings from a Prospective Cohort of 533 Consecutive Patients Selected for Cytoreductive Surgery. Annals of Surgical Oncology. 2016;23(4):1261-70.
-
Dedrick RL, Myers CE, Bungay PM, DeVita VT, Jr. Pharmacokinetic rationale for peritoneal drug administration in the treatment of ovarian cancer. Cancer Treat Rep. 1978;62(1):1-11.
-
Jacquet P, Sugarbaker PH. Peritoneal-plasma barrier. Cancer Treat Res. 1996;82:53-63.
-
Tamura K, Kitayama J, Saga Y, Takei Y, Fujiwara H, Yamaguchi H, et al. Combined Intraperitoneal and Systemic Chemotherapy for Peritoneal Metastases: Drug Delivery Concepts, Pharmacokinetics, and Clinical Applications: A Narrative Review. Pharmaceutics. 2026;18(2).
-
Hildebrandt B, Wust P, Ahlers O, Dieing A, Sreenivasa G, Kerner T, et al. The cellular and molecular basis of hyperthermia. Crit Rev Oncol Hematol. 2002;43(1):33-56.
-
Löke DR, Helderman R, Franken NAP, Oei AL, Tanis PJ, Crezee J, et al. Simulating drug penetration during hyperthermic intraperitoneal chemotherapy. Drug Deliv. 2021;28(1):145-61.
-
Goodman MD, McPartland S, Detelich D, Saif MW. Chemotherapy for intraperitoneal use: a review of hyperthermic intraperitoneal chemotherapy and early post-operative intraperitoneal chemotherapy. J Gastrointest Oncol. 2016;7(1):45-57.
-
Valle SJ, Alzahrani NA, Liauw W, Sugarbaker PH, Bhatt A, Morris DL. Hyperthermic Intraperitoneal Chemotherapy (HIPEC) Methodology, Drugs and Bidirectional Chemotherapy. Indian J Surg Oncol. 2016;7(2):152-9.
-
Sugarbaker PH. Peritonectomy procedures. Ann Surg. 1995;221(1):29-42.
-
Margioula-Siarkou C, Almperis A, Papanikolaou A, Laganà AS, Mavromatidis G, Guyon F, et al. HIPEC for gynaecological malignancies: A last update (Review). Med Int (Lond). 2023;3(3):25.
-
Lei Z, Wang Y, Wang J, Wang K, Tian J, Zhao Y, et al. Evaluation of Cytoreductive Surgery With or Without Hyperthermic Intraperitoneal Chemotherapy for Stage III Epithelial Ovarian Cancer. JAMA Netw Open. 2020;3(8):e2013940.
-
Karanikas M, Kofina K, Kyziridis D, Trypsianis G, Kalakonas A, Tentes AA. HIPEC as Up-Front Treatment in Locally Advanced Ovarian Cancer. Cancers (Basel). 2024;16(20).
-
Ghirardi V, De Felice F, D’Indinosante M, Bernardini F, Giudice MT, Fagotti A, et al. Hyperthermic intraperitoneal chemotherapy (HIPEC) after primary debulking surgery in advanced epithelial ovarian cancer: Is BRCA mutational status making the difference? Cancer Treat Res Commun. 2022;31:100518.
-
Lim MC, Chang SJ, Park B, Yoo HJ, Yoo CW, Nam BH, et al. Survival After Hyperthermic Intraperitoneal Chemotherapy and Primary or Interval Cytoreductive Surgery in Ovarian Cancer: A Randomized Clinical Trial. JAMA Surg. 2022;157(5):374-83.
-
van Driel WJ, Koole SN, Sikorska K, Schagen van Leeuwen JH, Schreuder HWR, Hermans RHM, et al. Hyperthermic Intraperitoneal Chemotherapy in Ovarian Cancer. N Engl J Med. 2018;378(3):230-40.
-
Huo YR, Richards A, Liauw W, Morris DL. Hyperthermic intraperitoneal chemotherapy (HIPEC) and cytoreductive surgery (CRS) in ovarian cancer: A systematic review and meta-analysis. European Journal of Surgical Oncology (EJSO). 2015;41(12):1578-89.
-
National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®): Ovarian Cancer Including Fallopian Tube Cancer and Primary Peritoneal Cancer (Version 2.2026). .
-
Filis P, Mauri D, Markozannes G, Tolia M, Filis N, Tsilidis K. Hyperthermic intraperitoneal chemotherapy (HIPEC) for the management of primary advanced and recurrent ovarian cancer: a systematic review and meta-analysis of randomized trials. ESMO Open. 2022;7(5):100586.
-
Aronson SL, Lopez-Yurda M, Koole SN, Schagen van Leeuwen JH, Schreuder HWR, Hermans RHM, et al. Cytoreductive surgery with or without hyperthermic intraperitoneal chemotherapy in patients with advanced ovarian cancer (OVHIPEC-1): final survival analysis of a randomised, controlled, phase 3 trial. Lancet Oncol. 2023;24(10):1109-18.
-
Ghirardi V, Trozzi R, Scanu FR, Giannarelli D, Santullo F, Costantini B, et al. Expanding the Use of HIPEC in Ovarian Cancer at Time of Interval Debulking Surgery to FIGO Stage IV and After 6 Cycles of Neoadjuvant Chemotherapy: A Prospective Analysis on Perioperative and Oncologic Outcomes. Ann Surg Oncol. 2024;31(5):3350-60.
-
Fagotti A, Costantini B, Fanfani F, Giannarelli D, De Iaco P, Chiantera V, et al. Hyperthermic Intraperitoneal Chemotherapy in Platinum-Sensitive Recurrent Ovarian Cancer: A Randomized Trial on Survival Evaluation (HORSE; MITO-18). J Clin Oncol. 2025;43(7):852-60.
-
Classe JM, Meeus P, Hudry D, Wernert R, Quenet F, Marchal F, et al. Hyperthermic intraperitoneal chemotherapy for recurrent ovarian cancer (CHIPOR): a randomised, open-label, phase 3 trial. Lancet Oncol. 2024;25(12):1551-62.
-
Jacquet P, Sugarbaker PH. Clinical research methodologies in diagnosis and staging of patients with peritoneal carcinomatosis. Cancer Treat Res. 1996;82:359-74.
-
Munoz-Zuluaga CA, King MC, Diaz-Sarmiento VS, Studeman K, Sittig M, MacDonald R, et al. Defining “Complete Cytoreduction” After Cytoreductive Surgery and Hyperthermic Intraperitoneal Chemotherapy (CRS/HIPEC) for the Histopathologic Spectrum of Appendiceal Carcinomatosis. Ann Surg Oncol. 2020;27(13):5026-36.
-
Chen D, Ma Y, Li J, Wen L, Zhang G, Huang C, et al. Risk factors for postoperative complications in patients undergoing cytoreductive surgery combined with hyperthermic intraperitoneal chemotherapy: A meta-analysis and systematic review. Int J Colorectal Dis. 2024;39(1):167.







